铁死亡及其研究进展
细胞程序性死亡是由基因决定的受到分子机制精密调控的细胞主动、有序的死亡方式,与生命体稳态的维持和疾病的发生密切相关,主要包括焦亡、坏死和自噬等形式。铁死亡是近几年发现的一种新的细胞程序性死亡方式,作为一种新的细胞死亡方式已成为科研人员瞄准的新方向。铁死亡这一概念最早在2012年由Dr. Dixon [1] 提出,它是一种铁依赖性的脂质过氧化、活性氧自由基大量累积所致的细胞死亡模式,受到多种细胞代谢途径的调控,其中包括氧化还原稳态、铁代谢、线粒体活性和氨基酸、脂质、糖的代谢,以及各种与疾病相关的信号途径。研究表明,铁死亡与器官损伤、神经退行性疾病、心血管疾病、炎症性疾病、癌症相关。特别是具有多重药物抗药性的癌细胞,尤其是处于间充质状态且易于转移的肿瘤细胞,非常容易发生铁死亡。因此,通过诱导和抑制铁死亡对其进行药理调节,在治疗耐药性癌症、缺血性器官损伤和其他与脂质过氧化密切相关的退行性疾病上具有巨大的潜力。

图1 细胞死亡的分类
铁死亡的生化特点: 铁死亡又名铁坏死,是一种与活性氧(reactive oxygen species, ROS)聚集有关的细胞死亡形式,其本质为铁蓄积和脂质过氧化。细胞抗氧化体系代谢异常时,Fe2+蓄积能够介导芬顿(Fenton)反应产生过量ROS(尤其是羟自由基),ROS与细胞膜上的多不饱和脂肪酸(polyunsaturated fatty acid, PUFA)发生过氧化反应,导致脂质双分子层稳定性遭到破坏,细胞膜解体,进而促进细胞铁死亡[1] 。

图3 铁死亡的主要途径
2.铁死亡主要途径
铁死亡可通过外源性或内源性途径诱发。
2.1外源性 (转运蛋白依赖) 途径
2.1.1氨基酸代谢—抑制胱氨酸/谷氨酸转运蛋白 [5]
System xc-是细胞内重要的抗氧化体系,该系统由2个亚基组成,SLC7A11和SLC3A2。SLC7A11负责主要的转运活性,对胱氨酸和谷氨酸有高度特异性,而 SLC3A2则作为伴侣蛋白。System xc-以1:1的比例用胞内谷氨酸来换取胞外的胱氨酸(Cys2),胱氨酸在谷氨酸半胱氨酸连接酶(GCL)和谷胱甘肽合成酶(GSS)的催化作用下合成谷胱甘肽(GSH)(GSH是膜脂修复酶-谷胱甘肽过氧化物酶(GPX4)的还原性辅因子)。抑制 System xc- 的活性会抑制胱氨酸的吸收,影响GSH的合成,继而导致膜脂修复酶GPX4活性降低,细胞抗氧化能力降低,从而促进铁死亡。
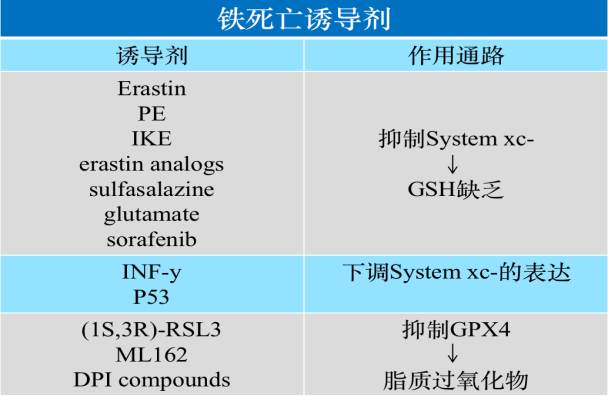
表2 目前已知的部分铁死亡诱导剂及作用通路
2.1.2铁代谢—转运蛋白与铁“超载” [6-7]
铁具有Fe2+和Fe3+两种氧化态。食物中Fe3+在肠道被还原为Fe2+后被小肠上皮细胞吸收。Fe2+在膜铁转运蛋白的作用下被运输至细胞外并被氧化为Fe3+,与转铁蛋白(transferrin, TF)(血清转铁蛋白或乳铁蛋白)结合形成TF-Fe3+复合物,经血液循环运输至各组织器官。Fe3+与细胞膜上的转铁蛋白受体(TFRC)结合进入细胞内后被金属还原酶STEAP3还原为Fe2+,然后通过二价金属转运蛋白1将Fe2+释放到胞质的动态铁池中。正常生理状态下,动态铁池可以维持铁平衡。
病理情况下,Fe 2+在细胞内集聚,发生哈伯-韦斯反应(Haber-Weiss)与Fenton反应,产生大量ROS,与细胞膜上的多不饱和脂肪酸PUFA发生一系列过氧化反应,生成脂质过氧化物,破坏细胞膜结构并引起细胞铁死亡。同时Fe2+作为多种代谢铁的积累是铁死亡过程中启动膜氧化的关键信号之一;TF通过TFRG介导铁摄取,FTH1/FTL (铁蛋白组件)通过自噬降解可以增加铁的水平并促进铁死亡。
SLC40A1介导的铁外流和外泌体介导的铁蛋白输出会抑制铁死亡。
2.2内源性 (酶调控) 途径
2.2.1脂质代谢—多不饱和脂肪酸PUFAs过氧化[8-9]
铁死亡的中心环节是铁依赖的脂质氧化代谢失调,多不饱和脂肪酸(PUFAs)是铁死亡中脂质过氧化物积累的关键物质。 正常情况下,PUFAs 是脂质代谢的重要底物,含有双烯丙基氢原子,尤其是花生四烯酸(arachidonoyl, AA)和肾上腺素酸(adrenoyl, AdA),易与ROS发生反应,引起脂质过氧化。当长链脂酰辅酶A合成酶4(ACSL4)催化游离的AA或AdA与辅酶A(coenzyme A, CoA)结合形成衍生物AA-CoA或AdA-CoA,然后被溶血卵磷脂酰基转移酶3(LPCAT3)酯化为膜磷脂酰乙醇胺(PEs),并经过脂氧合酶(ALOXs)或细胞色素P450氧化还原酶(POR)氧化后,就形成了有害的脂质过氧化产物,诱导细胞铁死亡。
乙酰辅酶A羧化酶(ACAC)介导的脂肪酸合成,脂质吞噬(Lipophagy)介导的脂肪酸释放,可诱导细胞内游离脂肪酸的积累,促进铁死亡。
2.2.2其他代谢途径
CoQ10能被铁死亡抑制蛋白1(ferroptosis suppressor protein 1, FSP1)还原来阻止脂质氧化进而抑制铁死亡。
NADPH能参与GSH-GPX4抗氧化系统的循环,其大量消耗将限制GSH-GPX4的抗氧化功能,诱导铁死亡。
硒是维持GPX4活性的一种必需的微量营养素,通过协同激活转录因子TFAP2c和Sp1调节GPX4的丰度和活性,在一定程度上抑制铁死亡以保护神经元。
NFE2L2可通过反式激活的方式调控包括铁代谢、GSH代谢以及抗ROS过程中的基因的表达进而限制铁死亡过程中的氧化损伤。
Vitamin E通过抑制ALOXs活性、减少脂质过氧化物的产生,从而抑制铁死亡。
p53可以通过下调Xc-系统组分SLC7A11的表达,抑制胱氨酸的摄取,从而诱导细胞铁死亡;同时p53可以抑制二肽基肽酶-4(dipeptidyl peptidase-4, DPP4)的活性,阻断Erastin诱导的铁死亡。
NRF2是维持细胞内氧化还原稳态的重要调控因子,通过p62-Keap1-NRF2途径上调参与铁和ROS代谢的多种基因(NQO1、HO1和FTH1)的表达,抑制细胞铁死亡。
3铁死亡在疾病治疗中的应用
铁死亡与癌症、衰老、神经退行性疾病、心肌病、中风、脑出血创伤性脑损伤、缺血
再灌注损伤和肾脏变性相关的病理细胞死亡有关。
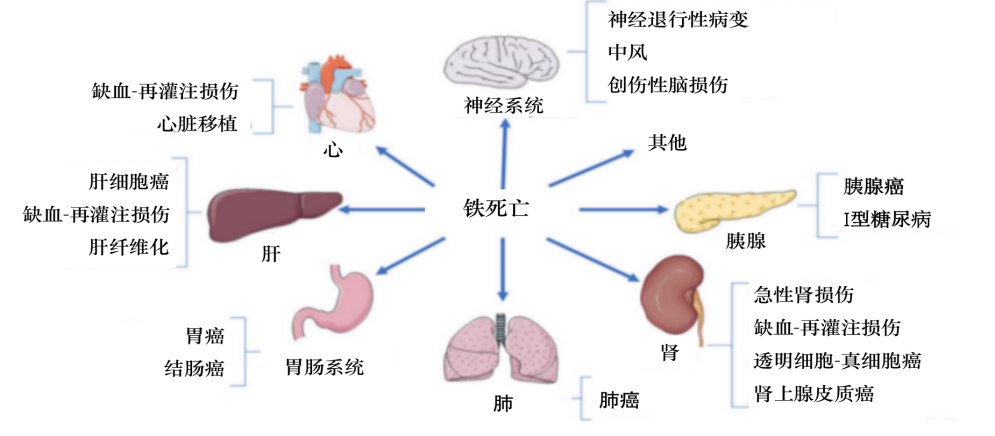
图5 铁死亡相关疾病
3.1 癌症
研究表明许多癌症相关基因和信号通路都能调控铁死亡,诱导癌细胞铁死亡对治疗癌症意义重大。对凋亡和常规癌症疗法抵抗的间充质干细胞和去分化的癌细胞,以及被称为“持续细胞”的癌细胞都对铁死亡诱导高度敏感。与正常细胞相比,癌细胞代谢比较旺盛,线粒体出现功能障碍,ROS积累较多,增加了癌细胞对铁死亡的敏感性。
卵巢癌:实验证实在卵巢癌中可通过TAZ-ANGPTL4-NOX2信号轴激活铁死亡抑制卵巢癌细胞的增殖。
结、直肠癌:细胞红蛋白(cytoglob, CYGB)是ROS的细胞调节剂,也是一种肿瘤抑制剂,能够促进细胞膜上的脂质过氧化进而抑制结直肠癌细胞的生长,过表达CYGB的结直肠癌细胞对RSL3和Erastin诱导的铁死亡更敏感,敲除Yes相关蛋白1基因YAP1可通过减轻ROS的产生降低结、直肠癌细胞对铁死亡的敏感性。
另外,癌症的治疗可以通过靶向氨基酸、脂质、铁代谢相关信号通路进行。
3.2 衰老和神经退行性疾病
在衰老和退行性疾病如帕金森病(Parkinson's disease, PD)、亨廷顿病和阿尔茨海默病(Alzheimer's disease, AD)的患者中检测到铁水平升高,其原因可能是随着年龄的增长,铁的代谢速率不断降低,导致机体铁过量和过氧化损伤,最终引起细胞死亡。
多种证据表明,GSH-GPX4抗氧化通路在AD和PD患者中均出现明显异常,使用抗氧化药物可以缓解AD与PD病理症状。
研究显示,使用铁死亡抑制剂能够保护帕金森病模型小鼠免受过氧化损伤。
大鼠海马切片培养的离体实验表明,铁死亡抑制剂ferrostatin-1可阻断谷氨酸诱导的神经元兴奋毒性细胞死亡。
遗传学研究一致证实,小鼠条件性缺失Gpx4会引起类似神经退行性病变的症状。
3.3缺血再灌注损伤
缺血再灌注损伤是一种无菌性炎症。器官或组织缺血一段时间后重新获得血液供应,但缺血性损伤不但没有减轻反而进一步加重,甚至出现更严重的细胞代谢功能障碍或结构破坏。在脑缺血-再灌注损伤中铁蓄积和脂质过氧化等现象与铁死亡一致,且这一现象可以被铁螯合剂或抗氧化剂抑制。
在小鼠心脏缺血-再灌注损伤模型中,在再灌注开始时给予抑制铁死亡的小分子化合物Liproxstatin-1能够增加线粒体内GPX4的含量,降低线粒体内ROS的产生,降低缺血性梗死面积并改善线粒体结构和功能。
在糖尿病大鼠心脏缺血-再灌注模型中发现, ROS与内质网应激相互联系是引发铁死亡的重要因素,其能够进一步造成心脏缺血-再灌注损伤。
在缺血-再灌注损伤小鼠模型、Gpx4全身敲除小鼠和叶酸诱导急性肾损伤小鼠模型中,铁死亡抑制剂已被证明可以减轻肾小管细胞死亡和急性肾功能衰竭。
肝细胞特异性Gpx4敲除小鼠出生不久即会死亡,但高水平的维生素E饮食可以弥补肝脏中GPX4的缺乏,使小鼠存活。
此外Liproxstatin-1(一种强效铁死亡抑制剂)能保护肝实质组织免受缺血-再灌注损伤。
3.4心脑血管疾病
发生脑卒中时,胞内脂质过氧化物及 Fe2+水平升高,而使用铁死亡抑制剂上调 GSH、GPX4或 System xc-水平均可减轻脑部损伤,这表明铁死亡介导了脑卒中。近年研究进一步发现,机体铁过载会降低动脉斑块的稳定性,使用铁螯合剂可缩小动脉斑块面积,减轻动脉粥样硬化的发展。心肌细胞凋亡是心力衰竭的重要病理变化,但研究表明心力衰竭过程中除细胞凋亡外还有铁死亡的参与,且两者独立并存。
4细胞铁死亡的检测
4.1形态学检测
超微形态学特征显示细胞膜断裂和出泡,线粒体变小、膜密度增高、线粒体脊减少或消失、线粒体外膜断裂,细胞核大小正常、但缺乏染色质凝聚。电镜下表现为细胞内线粒体变小及双层膜密度增高。
4.2生物学特征
*铁死亡的金指标:脂质过氧化物(Lipid peroxidation)
铁和活性氧(ROS)聚集,激活丝裂原活化蛋白激酶(mitogen-activatedprotein kinase,MAPK)系统,通过降低胱氨酸的摄取、耗竭谷胱甘肽,抑制ystem Xc-和增加还原型酰腺嘌呤二核苷酸磷酸氧化酶,释放花生四烯酸等介质。细胞内活性氧和脂质活性氧通过流式细胞术使用DCFH-DA、C11-BODIPY 和Liperfluo检测。
在细胞培养基中添加药物后,脂质过氧化物染色(Liperfluo)检测Lipid peroxidation,如为阳性结果,证明铁死亡发生;若在上述添加药物的细胞培养基中添加铁死亡抑制剂后,检测Lipid peroxidation为阴性结果,证明药物诱导的一定是铁死亡,而非其他死亡方式。
C11-BODIPY对自由基非常敏感,但不和脂质过氧化物反应,Liperfluo是目前唯一可以特异性检测脂质过氧化物的化合物。
4.3铁水平检测
可以使用PGSK探针,流式细胞术或共聚焦显微镜检测细胞内铁含量的细胞膜透性染料;或者使用Iron Assay Kit(试剂盒)检测细胞、组织中的铁水平。
实验原理:通常利用铁离子氧化状态的过渡性改变来进行各种化学反应。通过加入酸性缓冲液来释放铁离子,样品中的Fe2+可直接测定,或通过还原反应来测定铁元素(Fe2+和Fe3+)总含量。反应释放出的铁元素与生色团反应,生成与样品中的铁成正比的比色(593 nm)产物。
4.4细胞活性检测
可以使用MTT/CCK8法检测细胞活性。
4.5线粒体膜电位检测
可以使用TMRE荧光染料检测,TMRE能够特异性标记有活性的线粒体,是一种细胞膜可穿透性的,正电荷的,橘红色荧光染料。当线粒体膜电位降低时,荧光减弱。
实验原理:TMRE (tetramethylrhodamine, ethyl ester),中文名称叫做四甲基罗丹明乙酯,CAS号为115532-52-0,分子式为C26H27CIN2O7,分子量为515。TMRE是一种可渗透细胞膜的橘红色阳离子荧光探针,可在完整的线粒体中聚集,而去极化或非活跃性线粒体膜电位降低,导致TMRE积聚减少。检测时TMRE的最大激发波长为550nm,最大发射波长为575nm。正常状态下的线粒体内部存在大量的负电荷,作为阳离子探针的TMRE进入细胞内后可聚集在线粒体基质中,可发出明亮的橘红色荧光;当细胞发生凋亡时,线粒体膜电位丢失,线粒体通透性转换孔(MPTP)持续开放,TMRE被释放到细胞质中,线粒体内橘红色荧光强度明显下降。可用荧光显微镜、流式细胞仪、荧光酶标仪等仪器检测细胞,通过荧光信号的强弱来确定线粒体膜电位的变化和凋亡或坏死的发生。
4.6 qRT-PCR/Western blot检测
检测细胞内与铁死亡相关的因子的变化,例如COX-2,ACSL4,PTGS2,NOX1,GPX4和FTH1等,其中COX-2,ACSL4,PTGS2和NOX1在铁死亡细胞中表达上调;GPX4和FTH1在铁死亡细胞中表达下调。
参考文献:
[1]Dixon SJ, Lemberg KM, Lamprecht MR, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell, 2012, 149(5): 1060-1072.
[2]陈璐瑶,饶小珍.铁死亡的发生机制及相关疾病研究进展[J].生物学教学,2022,47(02):2-5.
[3]Jiang X, Stockwell BR, Conrad M.Ferroptosis: mechanisms, biology and role in disease.Nat Rev Mol Cell Biol, 2021,22(4):266-282.
[4]Daolin Tang, Xin Chen, Rui Kang, Guido Kroemer. Broadening horizons: the role of ferroptosis in cancer. Nat Rev Clin Oncol. 2021 Jan 29.
[5]Piani D, Fontana A. Involvement of the cystine transport system xc- in the Macrophage
-induced glutamate-dependent cytotoxicity to neurons. J Immunol, 1994, 152(7): 3578-3585.
[6] Outten FW, Theil EC. Iron-based redox switches in biology. Antioxid Redox Signal, 2009, 11(5): 1029-1046
[7] Gao M, Monian P, Quadri N, et al. Glutaminolysis and transferrin regulate ferroptosis. Mol Cel, 2015, 59(2): 298-308
[8]Yang WS, Kim KJ, Gaschler MM, et al. Peroxidation of polyunsaturated fatty acids by lipoxygenases drives ferroptosis. Proc Natl Acad Sci USA, 2016, 113(34): E4966-E4975
[9]Doll S, Proneth B, Tyurina YY, et al. ACSL4 dictates ferroptosis sensitivity by shaping cellular lipid composition. Nat Chem Biol, 2017, 13(1): 91-98



