【拓普课堂】浅谈动物模型与肠道微生物
肠道微生物(Gutmicrobiome)是生活在人类和其他动物消化肠道中的微生物群的所有基因组的总和[1]。肠道菌群在宿主的生存、健康和疾病中起了重要作用[2]。早在中医经典著作《黄帝内经》中就已提出肠胃对于人体的重要,李东垣深得《内经》之要,在《脾胃论》里指出“内伤脾胃,百病由生”。可见,肠菌对人体健康具有重要影响。随着现代对肠道菌群的研究,发现肠道菌群可直接参与宿主的神经调节、脂肪代谢、免疫调节等诸多方面。
动物模型
以动物建模有助于进行复杂的生物机制研究,且随着现代分子生物技术的蓬勃发展,高通量测序(Next-generation sequencing technology,NGS)技术的问世,使得肠道微生物的研究进入一个新的研究阶段。利用NGS技术获得庞大的数据信息,通过生物信息学手段,分析肠道微生物的多样性。利用统计分析,对大量数据进行多样性分析,比较给药前后肠道中主要菌群的差异性,解释药物可能的作用机制。对揭示肠道微生物对宿主的调节机制具有重要意义。
肠道微生物
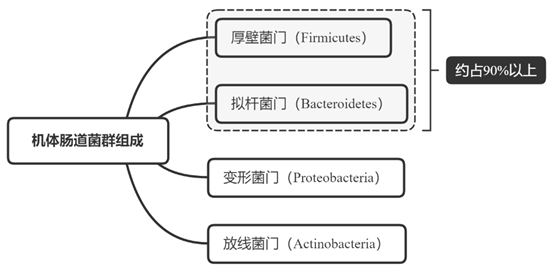
肠道菌群是寄居于宿主,并有益于宿主的一类微生物。肠道菌群在宿主体内有利于宿主方面的物质流动(参与碳水化合物代谢、参与脂肪代谢以及参与蛋白质代谢等)、能量流动(肠道内菌群的动力,是维持肠道微生态和生命活动的基础,并保持肠道菌群与宿主始终保持着能量交换和转运的关系。)以及基因流动(在肠道微生态中常常借助噬菌体和质粒在肠道微生物群中发生的基因交互)。
动物模型与肠道微生物相互作用研究
一、炎症性肠病 (inflammatory bowel disease,IBD)
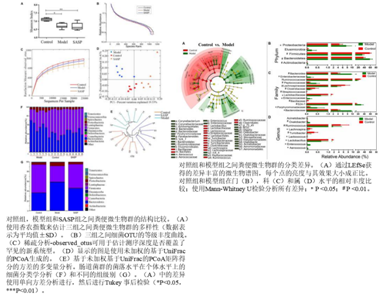
IBD模型通常是用2,4,6-三硝基苯磺酸(TNBS)联合乙醇灌肠致炎法,Haihui Zheng[3]等人通过对照组(用乙醇+盐水处理),模型组(用TNBS-乙醇+盐水处理)和SASP组(用TNBS-乙醇+SASP处理)研究肠道菌群的影响机制。研究基于分类学分析结果发现,模型组的Firmicutes比例降低,Proteobacteria和Bacteroidetes升高。给药治疗后(SASP组)可以增加Firmicutes的水平,降低Proteobacteria和Bacteroidetes的水平,从而将实验性结肠炎大鼠的肠道组成调节至与对照组相似的水平。
二、肿瘤疾病
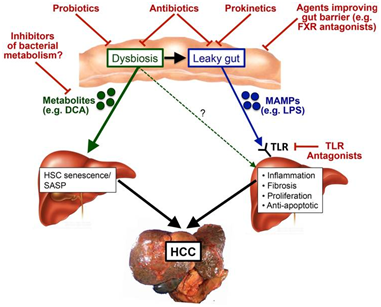
在DEN诱发肝癌的大鼠模型中,利用含有Streptococcus thermophiles,Bifidobacteriumbreve,Bifidobacterium longum,Bifidobacterium infantis,Lactobacillus acidophilus,Lactobacillus plantarum,Lactobacillus paracasei的制剂可以减轻肠生态失调,改善肠道炎症和肝肿瘤生长和多样性降低[4]。在皮下移植小鼠模型中,益生菌混合物Prohep(包含Lactobacillus rhamnosusGG,Escherichia coliNissle 1917)可以减少了肿瘤的大小和重量。
Jun Li[5]发现肠道菌群组成向有益细菌(Prevotella and Oscillibacter)的转移,以及这些细菌产生的抗炎介质,降低了肿瘤中Th17细胞的水平,从而限制了肿瘤的生长[6]。
三、糖尿病
HFD/STZ诱发糖尿病对肠道菌群有显著转变,其中可以降低Bacteroidetes和Proteobacteria,并且能够增加Firmicutes[7]。Qian Zhang等[8]人发现Lachnospiraceae_UCG-005,Lachnospiraceae_UCG-010,Oscillibacter,Ruminococcaceae_UCG-010,Anaerovorax,Kurghia,Bilophila,和Anaerotruncus(P <0.01)等有关的属与血糖水平升高有密切关系。

小结
由于大部分药物都是通过口服给药,肠道菌群会优先与药物成分相互作用。所以了解肠道菌群的代谢与药物治疗疾病的过程尤其重要。从某种意义上,中药是通过调节肠道菌群和人体的整体环境来治疗疾病。无论是健康或者是病理状态下人体生理代谢均受到肠道菌群结构变化的影响。通过建立相应的动物模型,实现体内菌群差异变化与体内内源性成分的关联具有重要意义。了解此类机制,可能会开发出新的突破性治疗方法,对阐明药物的作用机制与物质基础提供新的理论依据。
参考文献
[1] Kau A L, Ahern P P, Griffin N W, et al. Human nutrition, the gut microbiome and the immune system[J]. Nature,2011,474(7351):327-336.
[2] Albenberg L G, Wu G D. Diet and the Intestinal Microbiome: Associations, Functions, and Implications for Health and Disease[J]. Gastroenterology,2014,146(6):1564-1572.
[3] Zheng H, Chen M, Li Y, et al. Modulation of Gut Microbiome Composition and Function in Experimental Colitis Treated with Sulfasalazine[J]. Frontiers in Microbiology,2017,8.
[4] Zhang H L, Yu L X, Yang W, et al. Profound impact of gut homeostasis on chemically-induced pro-tumorigenic inflammation and hepatocarcinogenesis in rats[J]. Journal of Hepatology,2012,57(4):803-812.
[5] Li J, Sung C Y J, Lee N, et al. Probiotics modulated gut microbiota suppresses hepatocellular carcinoma growth in mice[J]. Proc Natl Acad U S A,2016,113(9):E1306.
[6] Yu, Le-Xing, Schwabe, et al. The gut microbiome and liver cancer: mechanisms and clinical translation[J]. Nature reviews. Gastroenterology & hepatology,2017.
[7] Hildebrandt M A, Hoffmann C, Sherrill Mix S A, et al. High-fat diet determines the composition of the murine gut microbiome independently of obesity.[J]. Gastroenterology,2009,137(5):1716-1724.
[8] Zhang Q, Xiao X, Li M, et al. Vildagliptin increases butyrate-producing bacteria in the gut of diabetic rats[J]. Plos One,2017,12(10):e184735.



